Como a guerra química travada nos hospitais está acelerando a evolução das bactérias — e por que o futuro da desinfecção pode ser biológico.
Autor: Henrique Klein
Dirigido a: Comissões de Controle de Infecção Hospitalar (CCIH), Infectologistas, Enfermeiros de Controle de Infecções, Diretores de Hospitais, Gerentes de Hotelaria.
Desde que Charles Darwin formulou a teoria da seleção natural, entendemos que os organismos mais aptos sobrevivem e se reproduzem, moldando o mundo vivo à sua volta. Hoje, essa lógica evolutiva se aplica também aos microrganismos que habitam nossos hospitais.
Em um contexto onde protocolos agressivos de desinfecção se tornaram rotina, as bactérias estão “aprendendo” a resistir às pressões químicas que deveriam eliminá-las. Através da seleção ecológica, da resistência cruzada e da tolerância induzida por stress ambiental, microrganismos comuns podem evoluir para patógenos multirresistentes, criando uma verdadeira “tempestade perfeita” para a saúde humana.
Este artigo explora como nossas práticas modernas de higiene, embora bem-intencionadas, podem inadvertidamente acelerar a evolução bacteriana, destacando soluções emergentes e inteligentes, como tecnologias biológicas e sistemas de inteligência de gestão de limpeza , para enfrentar essa ameaça de forma mais estratégica e eficaz.
A lógica parecia robusta: ao contrário dos antibióticos, que atuam como "chaves" moleculares precisas que as bactérias podem alterar, os desinfetantes são como "marretas". São aplicados em concentrações massivas – centenas ou milhares de vezes acima da Concentração Inibitória Mínima (MIC) – e atacam indiscriminadamente múltiplas estruturas celulares vitais, como membranas e proteínas. Como poderia uma bactéria, perguntávamo-nos, desenvolver defesa contra um ataque tão brutal e generalizado?
Preparem-se para uma verdade inconveniente: essa lógica está profundamente falha. Um conjunto crescente e alarmante de investigações científicas detalhadas, incluindo as anexadas a este documento, sugere que nossa "guerra química" contra os micróbios em superfícies não só está falhando em nos proteger adequadamente, como está ativamente engenheirando a próxima onda de patógenos multirresistentes.
Este artigo irá dissecar, com base em evidências científicas robustas, como nossa obsessão pela desinfecção está criando uma "tempestade perfeita" para a Resistência Antimicrobiana (RAM), através de três mecanismos interligados e profundamente preocupantes que estão operando agora mesmo nas superfícies que limpamos todos os dias.
Mecanismo 1: O "Exterminador Seletivo" – Filtragem Ecológica de Espécies Super-Resistentes O primeiro golpe na nossa confiança vem da constatação de que a desinfecção intensiva não leva à esterilidade. Ela apenas remodela a comunidade microbiana, muitas vezes para pior.
Um estudo marcante conduzido por Shanshan Ye e colegas do Centro Provincial de Controle e Prevenção de Doenças de Jiangsu, China (publicado em 2025), investigou as comunidades bacterianas em botões de elevador em diferentes ambientes: hospitais gerais, um hospital de doenças infecciosas, hotéis gerais e hotéis designados para quarentena COVID-19. Estes últimos implementaram regimes de desinfecção brutais, com limpeza após cada uso, totalizando pelo menos 20 desinfecções diárias, usando uma combinação de etanol a 75% e desinfetantes à base de cloro a 1000 mg/L.
O resultado? Longe da erradicação, ocorreu uma substituição ecológica dramática. Os hotéis em quarentena apresentaram uma diversidade microbiana significativamente menor (tanto alfa-diversidade quanto beta-diversidade). A flora cutânea comum, como o gênero Cutibacterium (especificamente Cutibacterium acnes), que dominava nos outros locais, foi praticamente eliminada. Em seu lugar, prosperaram patógenos ambientais notoriamente robustos, com os gêneros Pseudomonas, Xanthomonas (especificamente Xanthomonas campestris) e Burkholderia tornando-se dominantes (ver Figura 1B de Ye et al., 2025).
Esse fenômeno de "filtragem" – onde a pressão química elimina os competidores fracos e deixa o campo livre para os mais fortes – é corroborado por David Lehman e colegas da Universidade da Virgínia (publicado em 2025). Eles avaliaram a tolerância in vitro à clorexidina (CHX), um antisséptico onipresente em ambientes de saúde (usado em sabonetes para lavagem das mãos em UTIs), em diversas espécies de Klebsiella isoladas de pacientes e do ambiente hospitalar (ralos de pias, etc.).
De forma alarmante, a espécie que exibiu as MICs mais elevadas (maior tolerância) não foi o patógeno clínico mais comum, Klebsiella pneumoniae sensu stricto (MIC90 = 32 µg/mL), mas sim Klebsiella quasipneumoniae (MIC90 = 64 µg/mL), uma espécie mais frequentemente associada a nichos ambientais (ver Figura 1 de Lehman et al., 2025). K. quasipneumoniae mostrou tolerância significativamente maior que K. pneumoniae sensu stricto (p=0,004) e K. oxytoca (p=0,002). Outras espécies ambientais como Klebsiella variicola (MIC90 = 32 µg/mL) também mostraram tolerâncias elevadas. Em contraste, Escherichia coli, frequentemente usada como controle, apresentou MICs significativamente mais baixas (MIC90 = 8 µg/mL).
Implicação Chocante nº 1: Seus rigorosos protocolos de limpeza podem estar fazendo mais mal do que bem. Ao invés de criar um santuário estéril, estão funcionando como um campo de seleção darwiniana, eliminando bactérias comensais e selecionando ativamente espécies como Serratia marcescens (conhecida por sua alta tolerância intrínseca à CHX), Pseudomonas aeruginosa e certas Klebsiella ambientais (K. quasipneumoniae, K. variicola) que são inerentemente mais "casca grossa". Esses sobreviventes formam novos e persistentes reservatórios em locais úmidos como ralos e sifões, precisamente onde podem adquirir e trocar genes de resistência a antibióticos clinicamente devastadores, como as carbapenemases (blaKPC).
Mecanismo 2: A "Autoestrada Genética" – Como os Desinfetantes Aceleram a Propagação da Resistência Se selecionar espécies naturalmente mais fortes é preocupante, o que dizer de criar ativamente resistência em bactérias anteriormente suscetíveis? É aqui que entra o verdadeiro perigo do "uso incorreto" ou, mais precisamente, da exposição inevitável a concentrações subletais.
Seja por diluição inadequada, aplicação em superfícies porosas, resíduos que persistem no ambiente ou a diluição natural que ocorre nas águas residuais hospitalares e municipais, as bactérias frequentemente encontram desinfetantes em doses que não as matam, mas as desafiam. Essa exposição subletal é o catalisador perfeito para a evolução da resistência adquirida através de mecanismos genéticos:
Resistência Cruzada (O Mecanismo "Dois em Um"): A bactéria desenvolve ou ativa um mecanismo de defesa que, fortuitamente, funciona tanto contra o desinfetante quanto contra um ou mais antibióticos. Como detalhado por Ayodeji Osunla e colegas da Universidade de Saskatchewan (2025) e Marco Krewing e colegas da BODE Chemie GmbH (2024), um dos principais intervenientes aqui são as bombas de efluxo multidrogas (MDR). Estas são proteínas na membrana bacteriana que funcionam como bombas de porão, expulsando ativamente substâncias tóxicas.
Estudos mostram que a exposição a desinfetantes comuns como os Compostos de Amônio Quaternário (QACs) – presentes em inúmeros produtos – ou a Clorexidina (CHX) pode induzir a expressão ou selecionar mutações nessas bombas (pertencentes a famílias como RND, SMR, MFS, MATE, ABC).
O problema crítico: essas mesmas bombas são promíscuas. A bomba AcrAB-TolC, por exemplo, prevalente em Gram-negativos como E. coli e Klebsiella, expulsa QACs, mas também é notoriamente eficaz para expulsar fluoroquinolonas (ex.: ciprofloxacina), tetraciclinas e cloranfenicol. Outras bombas induzidas por CHX podem expulsar tetraciclina, gentamicina e meropenem. Osunla et al. (2025) citam especificamente estudos onde a exposição a QACs induziu resistência cruzada a ampicilina, cloranfenicol e norfloxacina em E. coli.
Co-Resistência (O Gene "Cavalo de Troia"): Este é talvez o mecanismo mais insidioso. Aqui, os genes que conferem resistência ao desinfetante (por exemplo, genes qacE ou qacEΔ1 que codificam bombas de efluxo específicas para QACs) residem fisicamente no mesmo Elemento Genético Móvel (MGE) – como um plasmídeo ou um integron de classe 1 – que também carrega um arsenal de Genes de Resistência a Antibióticos (ARGs).
O estudo de Bahar Onaran Acar e colegas da Universidade de Ancara (2025) ilustra isso dramaticamente. Eles investigaram isolados de Staphylococcus aureus já conhecidos por serem resistentes a antibióticos críticos (MRSA, resistentes à Vancomicina e/ou Linezolida) e isolados de Enterococcus resistentes à Vancomicina (VRE). Descobriram uma correlação assustadora: esses isolados multirresistentes a antibióticos também exibiam altas taxas de resistência a desinfetantes (particularmente Triclosan, com 81% de resistência) e a metais pesados (Cobalto 83%, Níquel 86%, e 100% a Zinco e Chumbo). Os autores sugerem que essa co-ocorrência está ligada ao uso desses compostos na pecuária e à presença dos genes de resistência nos mesmos MGEs.
Ye et al. (2025) forneceram a prova ambiental definitiva. Nos hotéis de quarentena hiper-desinfetados, eles não encontraram apenas uma mudança na composição de espécies, mas também uma abundância significativamente maior de DRGs (genes de resistência a desinfetantes), ARGs (genes de resistência a antibióticos) e MGEs (os "veículos" genéticos que os transportam) nas superfícies dos botões de elevador. Os genes de efluxo AcrAB, OprF e TolC estavam particularmente elevados. As estirpes de Staphylococcus aureus isoladas desses hotéis também mostraram uma Concentração Bactericida Mínima (MBC) mais elevada para desinfetantes à base de cloro (250 mg/L vs 200 mg/L nos outros locais) (ver Figura 3 de Ye et al., 2025).
Para adicionar insulto à injúria, Osunla et al. (2025) destacam investigações que sugerem que a própria presença de QACs em concentrações ambientais pode aumentar a frequência da Transferência Horizontal de Genes (HGT) – o processo pelo qual as bactérias compartilham esses MGEs carregados de resistência. Desinfetantes à base de cloro também demonstraram promover a HGT mediada por plasmídeos. Estamos, literalmente, lubrificando as engrenagens da evolução da resistência.
Implicação Chocante nº 2: Seu frasco de spray desinfetante pode ser uma arma de dois gumes. Cada utilização, especialmente se não for perfeita, não só seleciona bactérias resistentes ao próprio produto, como também co-seleciona resistência a um cocktail de antibióticos. Pior ainda, pode estar acelerando ativamente a troca desses genes de resistência entre a comunidade bacteriana, incluindo patógenos perigosos.
Mecanismo 3: O "Escudo de Stress Invisível" – Como o Ambiente Real Anula a Potência do Seu Desinfetante Aqui reside a revelação mais contraintuitiva e potencialmente devastadora para nossas práticas atuais. Mesmo que uma bactéria não possua resistência intrínseca (Mecanismo 1) ou adquirida (Mecanismo 2), será que a alta concentração do desinfetante garante sua morte? A resposta, surpreendentemente, é: nem sempre.
A investigação pioneira de Samantha McCarlie e Robert Bragg da Universidade do Estado Livre, África do Sul (publicada em 2024), desafia nossa compreensão fundamental da suscetibilidade a biocidas. Usando análises transcriptômicas (RNA-Seq), eles examinaram quais genes eram ativados ou desativados em uma estirpe de Serratia resistente a QAC (Serratia sp. HRI) quando exposta ao desinfetante DDAC (um QAC) e a um produto comercial à base de DDAC (Virukill™).
A descoberta central foi a regulação maciça de vias metabólicas ligadas à resposta ao stress, especificamente o aumento do transporte de metionina e a síntese de poliaminas (como putrescina e espermidina). As poliaminas são moléculas ancestrais conhecidas por desempenharem papel crucial na proteção das células bacterianas contra vários tipos de stress ambiental. A metionina é um precursor chave para sua síntese via S-adenosilmetionina (SAM).
Mas a genialidade do estudo veio a seguir. Os pesquisadores levantaram a hipótese: se a exposição ao QAC ativa uma resposta ao stress, o que acontece se a bactéria já estiver "stressada" por outros fatores antes de encontrar o desinfetante? No mundo real, fora da placa de Petri ideal, as bactérias estão constantemente sob stress:
- Stress osmótico: em superfícies secas ou com resíduos de sabão.
- Stress de pH: em ambientes ácidos ou alcalinos.
- Stress oxidativo: simplesmente pela exposição ao oxigênio do ar ou resíduos de outros agentes.
- Stress térmico: variações de temperatura.
- Stress de envelope: danos à membrana celular por outros agentes.
Eles testaram essa hipótese expondo tanto a estirpe resistente Serratia sp. HRI quanto uma estirpe de referência suscetível (Serratia marcescens ATCC 13880) a sete tipos diferentes de stress ambiental antes de medir sua MIC para o desinfetante Virukill™.
Os resultados são um soco no estômago para qualquer profissional de controle de infecções: em ambas as estirpes (resistente e suscetível), a exposição prévia a quase todos os tipos de stress levou a um aumento dramático e estatisticamente significativo na MIC do desinfetante. Na estirpe resistente HRI, o pré-stress osmótico e oxidativo levou a um aumento de 60 vezes na MIC (ver Figura 4 de McCarlie & Bragg, 2024). Na estirpe ATCC, o aumento foi também significativo para todos os stressores, exceto o frio (ver Figura 5 de McCarlie & Bragg, 2024).
Implicação Chocante nº 3: As MICs reportadas pelos fabricantes, e nossa confiança nas "altas concentrações", são baseadas em testes de laboratório que não refletem a realidade fisiológica das bactérias nas nossas instalações. Uma bactéria em uma superfície "real" não é uma célula ingênua; é frequentemente uma sobrevivente já "preparada para a batalha" pela resposta ao stress. Esse "escudo fisiológico", provavelmente mediado por poliaminas, pode tornar concentrações de desinfetante que consideramos "instantaneamente letais" em meramente subletais, dando à bactéria a oportunidade de sobreviver, adaptar-se e, potencialmente, adquirir resistência genética permanente. Isso ecoa o conceito de "tolerância" vs. "resistência" discutido por Krewing et al. (2024), mas com uma implicação prática devastadora: a tolerância induzida pelo stress ambiental pode ser suficiente para anular a eficácia do nosso protocolo no mundo real.
Conclusão: Repensar ou Perecer – A Urgência de uma Nova Estratégia de Higiene A evidência acumulada é forte demais para ser ignorada. Nossa abordagem simplista e agressiva à desinfecção de superfícies, impulsionada por um medo compreensível, mas talvez mal direcionado, está saindo pela culatra de forma espetacular. Estamos travando a guerra errada, com armas que fortalecem o inimigo.
Resumindo os Pontos Críticos:
- Seleção Ecológica: Estamos eliminando a concorrência microbiana "normal" e criando nichos perfeitos para patógenos ambientais intrinsecamente mais tolerantes a biocidas, que por sua vez servem de reservatório para genes de resistência a antibióticos.
- Aceleração Genética: Estamos usando desinfetantes que, por meio de resistência cruzada e co-resistência, selecionam diretamente para resistência a antibióticos críticos. Pior, podemos estar aumentando a taxa de compartilhamento desses genes de resistência na comunidade microbiana.
- Priming Fisiológico: Subestimamos drasticamente a resiliência das bactérias no mundo real. A resposta ao stress ambiental onipresente pode conferir uma tolerância transitória, mas clinicamente significativa, que anula a eficácia das concentrações de desinfetante que usamos.
A distinção entre "resistência" genética e "tolerância" fisiológica torna-se um ponto acadêmico perigoso quando confrontado com a realidade operacional. Se uma bactéria sobrevive ao seu protocolo, seja por um gene qac em um plasmídeo ou por um escudo de poliaminas induzido pela secura, o resultado prático é o mesmo: falha na desinfecção, risco de transmissão e mais pressão seletiva para a evolução da resistência.
O que fazer? A resposta não é abandonar a higiene, mas sim revolucioná-la:
- Questionar a frequência e intensidade dos protocolos. A desinfecção constante é sempre necessária, ou estamos exagerando?
- Diversificar agentes desinfetantes. A dependência excessiva de QACs e CHX pode ser problemática. Estratégias de rotação ou combinação de desinfetantes com diferentes modos de ação podem ser mais eficazes.
- Investir em tecnologias biológicas emergentes, como as desenvolvidas pela Biont Biotecnologia, que oferecem alternativas seguras e eficazes para reduzir a pressão seletiva sobre microrganismos.
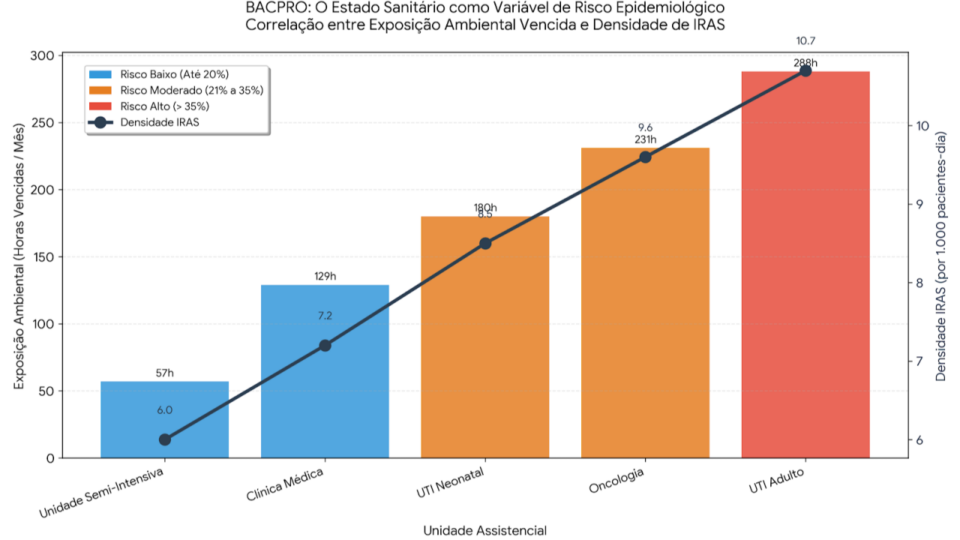
- Integrar sistemas de gestão de limpeza inteligentes, como a plataforma BACPRO, permite monitorar e otimizar protocolos em tempo real, garantindo eficácia e segurança.
- Desenvolver melhores métodos de teste. Avaliar desinfetantes contra bactérias "stressadas" e em biofilmes, e não apenas em suspensões planctônicas ideais, é essencial para refletir a realidade operacional.
- Implementar vigilância integrada. Monitorar não apenas patógenos clínicos, mas também reservatórios ambientais e genes de resistência que eles carregam (DRGs, ARGs, MGEs), permitindo intervenções mais precisas.
- Considerar o uso de tecnologias complementares, como sistemas de desinfecção UV-C oferecidos pela Elroi Tecnologia Hospitalar, que podem reforçar os protocolos convencionais sem comprometer o microbioma natural.
Estamos em uma encruzilhada crítica. Continuar no caminho atual da "guerra química total" contra micróbios em superfícies é, paradoxalmente, fortalecer o inimigo a longo prazo. É hora de admitir que o protocolo, como o conhecemos, falhou. Precisamos de uma abordagem mais inteligente, ecológica e, francamente, mais humilde na gestão do microbioma ao nosso redor, antes que criemos monstros que não conseguimos controlar.
Partilhe este artigo. Discuta-o na sua próxima reunião da CCIH. Questione o status quo. O futuro da eficácia dos antimicrobianos pode depender disso.